Dr. Csizmadia Tamás zalai származású sejtbiológus egyike a Nemzeti Kutatási, Fejlesztési és Innovációs Hivatal (NKFI) által 2020-ban meghirdetett fiatal kutatói (PD-OTKA) pályázat nyerteseinek. Az elnyert támogatás összege 25 millió forint, amely 3 évre szól.
Kutatásai során arra a kérdésre keresi a választ, hogy a mirigysejtekben megtermelődő, ámbár feleslegessé váló váladékszemcsék a kiürülés helyett milyen módon jelölődnek ki a lebontásra. A kutatásokhoz ecetmuslica lárvák és fiatal bábok nyálmirigyeit használja.
Korábban már írtunk az ELTE Anatómiai, Sejt- és Fejlődésbiológiai Tanszék egyetemi adjunktusáról, Dr. Csizmadia Tamásról, akinek a kutatásait az elkövetkező 3 évben az NKFI posztdoktori ösztöndíja finanszírozza.
A Keszthelyen született kutató, munkája során ecetmuslicák segítségével fogja feltárni és vizsgálni azokat a géneket, melyek közvetlenül szabályozzák a sejtekben maradó váladékszemcsék lebontását. A cél a folyamat jobb megértése, ezáltal mesterséges módon való indukálása a mirigysejtekben, mely hozzásegítheti az orvosokat a különféle emberi betegségek hatékonyabb megértéséhez és kezeléséhez is.

Dr. Csizmadia Tamás ellenőrzi a kísérleti állatok korát. Kutatásaik modellszervezeteit kicsi üvegcsövekben, kukoricaliszt alapú táptalajon tarják, ezáltal igen sokféle genetikai hátterű állat kis helyen könnyedén eltartható, tenyészthető
Fotó: Dr. Csizmadia Tamás
Mi a krinofágia?
– A krinofágia egy olyan sejtbiológiai folyamat, ami általánosan minden sejtben előfordul, amely valamiféle váladékot termel és ürít a környezetébe, különösen tehát a mirigysejtekre jellemző. Azonban a megtermelt anyagnak csak egy része fog ürülni az aktuális szükségleteknek megfelelően.
A krinofágia során a kiürítésre nem kerülő váladék úgynevezett váladékszemcsékbe (szekréciós granulumokba) csomagolva a sejtekben marad, majd ezek emésztőenzimeket tartalmazó sejtszervecskékkel (lizoszómákkal) egyesülnek. Ennek eredményeként a két sejtszervecske belső terében található komponensek (a lebontandó váladék és a lebontást végző emésztőenzimek) elkeverednek egymással, ezáltal történhet meg a kiürítésre nem került anyag sejten belüli lebontása, majd újra hasznosítása.
A krinofágia folyamatát már igen korán, 1966-ban, mintegy 55 évvel ezelőtt felfedezték, az azt szabályozó molekulák jó része azonban máig ismeretlen.
A doktori munkám során a szekréciós granulumok és lizoszómák egyesüléséhez szükséges molekuláris gépezet komponenseinek feltárását végeztem el az általunk a világon elsőként kifejlesztett, speciális módszerek segítségével – magyarázta Dr. Csizmadia Tamás.
A doktori fokozat megszerzése után folytatni szerette volna a krinofágia molekuláris mechanizmusának még alaposabb feltárását. Kezdetben ezért különféle sejten belüli jelátviteli utak jellegzetes komponenseit tesztelte, de az eredmények nem voltak meggyőzőek, ezért más irányú kutatásokba kezdett.
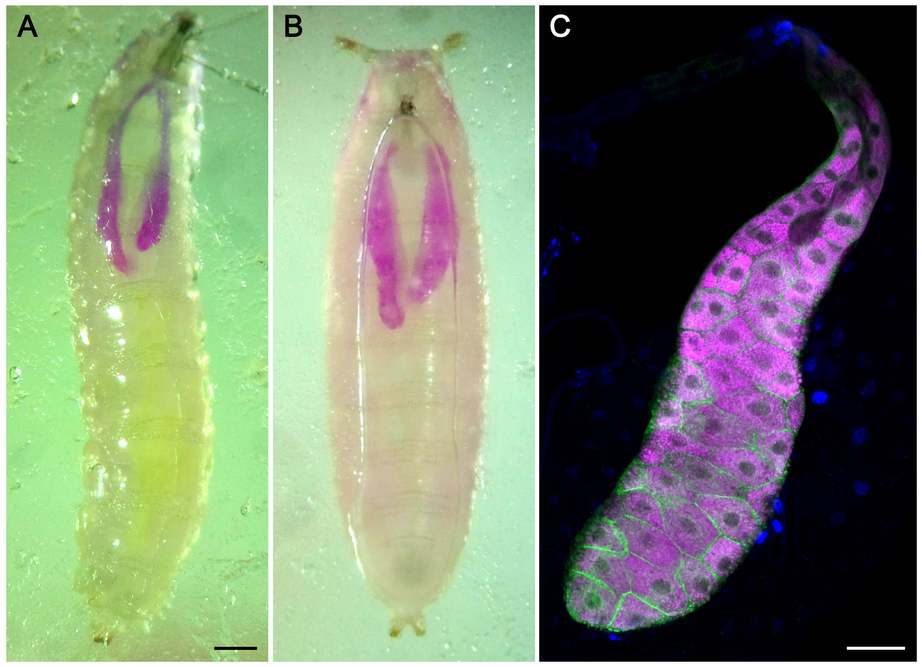
Ecetmuslica lárva (A) és fiatal báb (B) nyálmirigyében genetikai módszerekkel bíborvörös színű fehérje van túltermeltetve, amely az élő állatokban kirajzolja a szerveket. A C felvételen izolált nyálmirigy egyik lebenyének epifluoreszcens mikroszkópos képe látható
Fotó: Dr. Csizmadia Tamás
Muslicalárvák nyálmirigyeit vizsgálta
– 2019 nyarának közepén, egyik vasárnap délután leültem a számítógépem elé, hogy alaposan áttanulmányozzam a kutatásaimhoz kapcsolódó szakirodalmat. A legtöbb kutatóval ellentétben engem nem különösebben érdekeltek a legfrissebb publikációk, mivel tudtam, hogy azok közt semmilyen használhatót nem fogok találni. Már régóta bennem volt az a gondolat, mely szerint a régi (50′-es – 60′-as évektől egészen a 90′-es évek végéig) publikációkban nagyon sok olyan kutatási eredmény lapulhat meg, amely eddig nem kapott kellő mértékű figyelmet, illetve elfeledték azokat. Szép példája ennek a már említett, 1966-ban a nőstény patkányok agyalapi mirigyének tejelválasztást serkentő sejtjeiben felfedezett, majd 1972-ben az ecetmuslicák egyik rokonának (Drosophila pseudoobscura) lárvális nyálmirigyében is azonosított krinofágia. Ezt az alapvető sejtbiológiai folyamatot sokáig igen nehéz volt vizsgálni, mivel nem volt ismert olyan alkalmas vizsgálati modellrendszer, melyben a krinofágia intenzív módon működne. Ezért ez a sejtbiológiai folyamat idővel a feledés homályába merült. Dr. Juhász Gábornak, az ELTE Anatómiai, Sejt- és Fejlődésbiológiai Tanszék egyetemi tanárának és egyben az SzBK (Szegedi Biológiai Kutatóközpont) professzorának jutott eszébe legelőször, hogy a krinofágia folyamatát érdemes volna ecetmuslicák (Drosophila melanogaster) lárváinak nyálmirigyében vizsgálni, mivel abban a fejlődés során természetes módon aktiválódik a folyamat – részletezte.
– Az irodalom áttanulmányozása során tehát régi, de releváns publikációkat kerestem. Fontos megjegyezni, hogy ezeknek a megtalálása igencsak komoly kihívás, ezáltal nagyon sok türelmet és kitartást igényel. Néhány óra kutakodás után azonban sikerült rábukkannom egy régi, élesztőgombákkal (Saccharomyces cerevisiae) foglalkozó tanulmányra még 1998-ból, amiben leírtak egy krinofágiához hasonló folyamatban szereplő enzimet, ami eddig elkerülte a figyelmemet. Ez az enzim egy speciális, lebontásra kijelölő fehérjét képes kapcsolni más szabad, illetve sejtszervecskék felszínén megtalálható fehérjékre.
Ezek alapján eszembe jutott, hogy érdemes volna megvizsgálnom, vajon a muslicalárvák nyálmirigyében ki tudom-e mutatni a váladék granulumok felszínén ezt a lebontásra kijelölő fehérjét. Ez egy viszonylag egyszerű teszt volt.
Kezdetben semmit sem találtam, ezért aztán arra gondoltam, hogy több fejlődési (a bebábozódáshoz egyre közelebb eső) időpontban kellene megvizsgálnom a muslicalárvák nyálmirigysejtjeit.
Hatalmas meglepetés volt, mikor sikerült megpillantanom a keresett fehérjére utaló jelet a szekréciós granulumok felszínén a mikroszkópban, pontosan abban a fejlődési időpontban, amikor a granulumok lebontása időszerűvé válik (utóbbit már korábban kimutattam, ezért tudtam viszonylag időben pontosan behatárolni azt). A kapott eredmények megdöbbentőek voltak számomra, mert tudtam, ha ez ténylegesen így van, akkor ez egy igencsak komoly felfedezés lehet, mivel rendkívül újszerű és szokatlan. Az eredményeket megmutattam a tanszék vezetőjének, Dr. Lőw Péternek is, aki megerősítette a feltételezésemet. Nem sokkal később más, független vizsgálati módszerekkel is sikerült igazolnom a jelenséget.
Néhány héttel később kiderült, hogy a patkányok hasnyálmirigyének elektronmikroszkópos vizsgálata során a tanszékünk néhány munkatársa már a 90′-es évek elején kimutatta a már említett lebontásra kijelölő fehérjét bizonyos váladék granulumok felszínén, de mivel nem tudták értelmezni a jelenséget, így nem foglalkoztak vele, tehát nem került publikálásra. Ez pedig azt jelenti, hogy a lebontásra kijelölő fehérje jelenléte a váladékszemcsék felszínén nemcsak a muslicák sejtjeire lehet jellemző, de magasabb rendű szervezetek, a humán betegségek modellrendszeréül igen gyakran és sikeresen használt patkányok (Rattus rattus) megfelelő sejtjeire is. Mindez pedig a folyamat vizsgálatának igencsak komoly orvosbiológiai relevanciáját vetíti előre.
Megelőzhető lehet a halálos kimenetelű hasnyálmirigy-gyulladás?
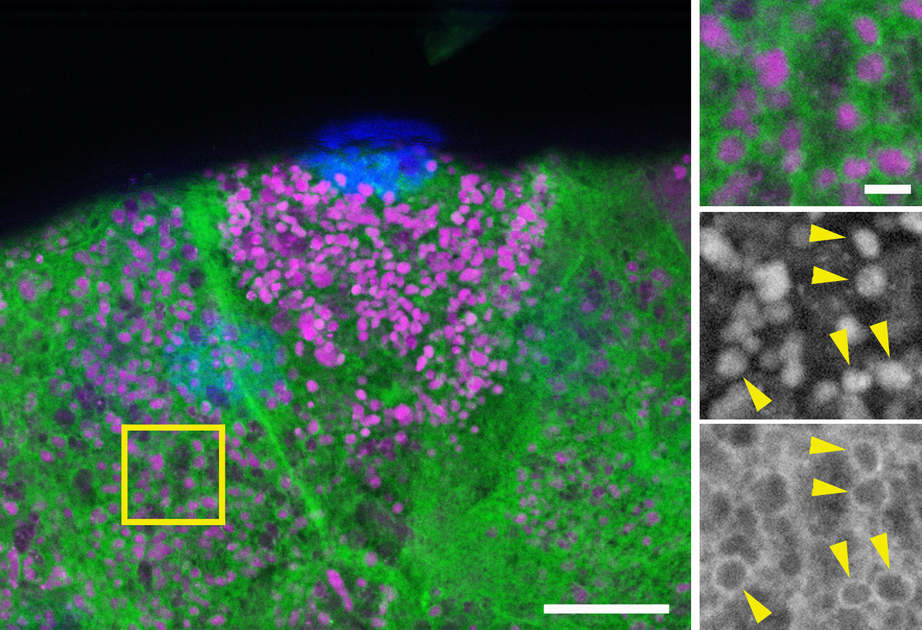
A halál csókja. A lebontásra kijelölő fehérje (zöld gyűrűk – jobb oldali legfelső és legalsó kép) megjelenése a váladékszemcsék (bíborvörös szemcsék – jobb oldali legfelső és középső kép) felszínéhez kötve. A lebontásra kijelölt váladékszemcséket a jobb oldali középső és alsó képen sárga nyilak jelölik. Eddigi kutatási eredményeik szerint ez a molekuláris cimke a váladékszemcséket a lebontási útra tereli a sejtben
Fotó: Dósa Anna
– A hasnyálmirigy emésztőenzimeket termelő sejtjeiben az enzimek inaktív (például trpiszinogén) formában váladékszemcsék belsejében várják, hogy kiürüljenek a sejtekből, majd a nyombélbe jutva ott aktiválódjanak. Amennyiben ezek a granulumok a kiürülés előtt intenzív módon egyesülnek a lizoszómákkal (krinofágia), akkor az azokban található lebontást végző molekulák képesek ideje korán aktiválni a tripszinogént, aktív és a sejten belül fokozott veszélyforrásnak tekinthető tripszinné alakítva, amely a sejtet belülről kezdi el megemészteni, ezáltal pedig a hasnyálmirigy sejt kipukkadással járó (necroticus) halálát okozva. Mindezek együttese és fokozódása pedig hozzájárulhat a hasnyálmirigy-gyulladás (pancreatitis) kialakulásához. Amennyiben megértjük a krinofágiát szabályozó molekulákat, mesterséges módon bele is avatkozhatunk a folyamatba, amely segítségével megelőzhető volna például a pancreatitis. Természetesen ehhez a betegséghez számos más tényező is hozzájárulhat, ezek közül csupán az egyik a krinofágia.
Ecetmuslicák segítségével idővel tehát jobban megérthetővé, kezelhetővé és talán megelőzhetővé válhat a sokszor halálos kimenetelű hasnyálmirigy-gyulladás – szögezte le a zalai sejtbiológus.
A posztdoktori OTKA pályázatot 2020 februárjában nyújtotta be, melynek sikeres eredményéről tavaly augusztusban értesült. A pályázat 2020 decemberétől indult és 2023 november végéig tart majd.
– A támogatás összege fedezi a munkabéremet, valamint vásárolhatok belőle a kutatásokhoz szükséges eszközöket, reagenseket. A pályázati pénz felhasználásának feltétele az, hogy a harmadik év végére legyen kézzel fogható eredménye a munkának, vagyis szülessen belőle minél színvonalasabb tudományos publikáció. A kutatás a Szegedi Biológiai Kutatóközpont (SzBK) munkatársaival szoros együttműködésben fog megvalósulni. Köszönettel tartozom az NKFI-nek a megítélt támogatásért, valamint Dr. Juhász Gábornak és Dr. Lőw Péternek a pályázat írása során nyújtott segítségükért, továbbá Kelemen Zsófiának a támogatásáért.
Forrás: zaol.hu